【前沿速遞】基于深度學習的人工智能在蛋白質結構預測領域正走向大眾

蛋白質是生命所必需的,理解它們的結構可以促進對其功能的機械性理解。幾十年來,研究人員使用x射線晶體學和低溫電子顯微鏡等實驗技術來確定蛋白質結構。但是這些方法既耗時又昂貴,而且有些蛋白質不適合此種技術分析。經過科學家們巨大的努力,到目前,大約有10萬種蛋白確定了三維結構,但這只是數十億已知蛋白質序列中的一小部分。要確定一個單一的蛋白質結構,用傳統的方法需要花費數月甚至數年的艱苦努力,這阻礙了蛋白質結構解析的覆蓋。需要精確的計算方法來解決這一差距,并使大規模的結構生物信息學成為可能。僅根據蛋白質的氨基酸序列預測其三維結構,即蛋白質折疊的結構預測問題,是50多年來一個重要的開放式研究問題。盡管最近取得了一些進展,但現有的方法還遠遠不能達到原子的精度,特別是在沒有同源結構的情況下。
近日,先后在Nature和Science雜志上發表的兩篇關于蛋白質結構深度預測的文章,讓科學家大受鼓舞。
7月15日,總部位于倫敦的DeepMind公司發布了其深度學習神經網絡AlphaFold 2的開源版本,并在《自然》雜志的一篇論文中描述了其方法(Jumper, J.et al. Nature https://doi.org/10.1038/s41586-021-03819-2 (2021)。DeepMind去年在科學界掀起了軒然大波,它展示了自己的軟件僅通過蛋白質序列(由DNA決定)就能準確預測許多蛋白質的結構。研究人員已經為這項挑戰工作了幾十年,AlphaFold 2在兩年一次的蛋白質預測活動CASP中表現非常好,該比賽的聯合創始人甚至宣稱,“在某種意義上,問題已經解決了”。
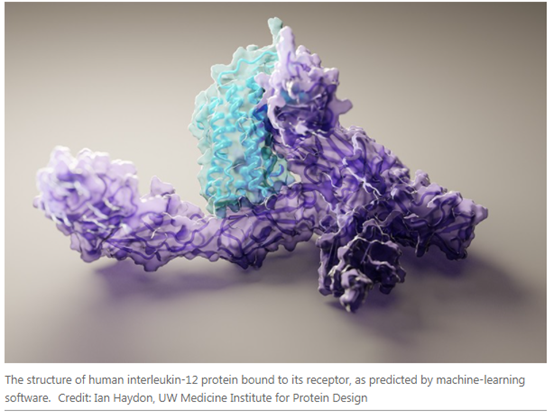
與此同時,受AlphaFold 2的啟發,一個學術團隊開發了自己的蛋白質預測工具,這款工具已經在科學家中越來越受歡迎。該系統被稱為RoseTTaFold,性能幾乎和AlphaFold 2一樣好,并在7月15日發表在《科學》雜志上的一篇論文中(Baek, M. et al.Science https://doi.org/10.1126/science.abj8754 (2021).)進行了描述。
基于人工智能的策略精準預測蛋白質的3D結構正變得成熟。科學家將廣泛使用能精確測定蛋白質3D形狀的軟件。
隨著高通量測序技術的不斷發展與完善,單組學研究也日趨成熟與完善,而整合多組學數據研究疾病靶點的工作方興未艾。近年來隨著新技術的不斷涌現,加快了多組學研究向定量化,高通量的發展,特別是在單細胞層次研究基因組學、轉錄組學、蛋白質組學和代謝組學,已成為人們發現生命化學物質基礎和深入了解其分子機制的新方向。通過對多組學數據的整合分析,有利于系統性地研究臨床發病機理、確認疾病靶點,發現生物標志物與進行疾病早期診斷,從而對個體化治療和用藥指導發揮重要作用。
為協助您更好的進行科學研究,2021年7月27日(周二)20:00-21:00,金開瑞特推出《多組學關聯分析 》線上直播課,歡迎各位老師掃碼進入直播間一起交流學習!


文章來源:
https://www.nature.com/articles/d41586-021-01968-y
最新動態
-
08.19
基因測序檢測—如何解讀基因密碼
-
12.06
重磅官宣| 2021年中國腫瘤標志物學術大會將于12月10-12日在沈陽隆重召開!
-
11.26
【院士主編大咖云集】第三屆國際醫學研究與發表高峰論壇即將開啟!
-
10.11
“C位”參展,金開瑞生物邀您共赴一場組學盛會!
-
09.26
2021| 第十一屆湖北植物生物學大會,即將開幕!
-
09.08
【會議通知】第二屆中南五省植物生理學會聯合學術年會
-
07.19
【前沿速遞】基于深度學習的人工智能在蛋白質結構預測領域正走向大眾
-
04.19
客戶文獻解讀| 光合作用相關蛋白在烤煙植株衰老過程中起關鍵作用:iTRAQ-PRM聯合研究
-
04.02
關于酵母雜交文庫構建及篩選你需要知道這些
-
01.15
官宣|高級職稱限兩項,2020年度國家自然科學基金項目指南已公布!










