1+1>2!深度解析RNA測序數(shù)據(jù)挖掘邏輯和后期實驗設計思路,輕松研獲10+ SCI
RNA,即核糖核酸,是生物體內(nèi)一種重要的生物大分子,它不僅在遺傳信息的傳遞和表達過程中扮演著關(guān)鍵角色,還在基因表達調(diào)控、細胞生長、分化、凋亡等生物學過程中發(fā)揮著重要作用。因此,對RNA的研究具有重要的科學意義和應用價值。
RNA可以根據(jù)其功能和結(jié)構(gòu)特點分為多個類別,其中包括mRNA(信使RNA)、tRNA(轉(zhuǎn)運RNA)、rRNA(核糖體RNA)以及非編碼RNA(ncRNA)。非編碼RNA又可以細分為多種類型,如長鏈非編碼RNA(lncRNA)、微小RNA(miRNA)、環(huán)狀RNA(circRNA)等。非編碼RNA作為基因組中不直接編碼蛋白質(zhì)的RNA分子,近年來受到了廣泛的關(guān)注,它在調(diào)控基因表達、維持染色質(zhì)結(jié)構(gòu)、影響細胞命運決定及參與多種生物學途徑中發(fā)揮著不可或缺的作用。本文將以非編碼RNA為例,深入講解RNA測序數(shù)據(jù)挖掘邏輯和后期實驗設計思路。
一般來說,非編碼RNA功能研究的主線包含3個主要步驟:
● 高通量篩選:采用高通量測序技術(shù)(如RNA-Seq)和相應的特異性數(shù)據(jù)庫進行高通量篩選,以獲取差異表達的候選RNA。
● 候選非編碼RNA的確定:在測序得到的非編碼RNA中,通常優(yōu)先選擇差異倍數(shù)大、表達水平高、且與研究方向相關(guān)的。
● 功能分析與驗證:基于生物信息學預測,設計實驗來驗證非編碼RNA的生物學功能。比如通過實時定量PCR、原位雜交等技術(shù),驗證RNA在特定樣本或條件下的表達情況。還可以通過RNA pull down、RIP、雙熒光素酶等實驗技術(shù),檢測與目標RNA相互作用的蛋白質(zhì)或RNA,進一步揭示RNA的生物學功能。然后在動物或細胞模型中驗證RNA的功能和調(diào)控機制,進一步確認其在生理和病理條件下的重要性。
實踐出真知,下面我們一起來看幾篇文獻案例加深下理解。
案例一
circSEPT9可作為TNBC潛在的生物標志物和治療靶點

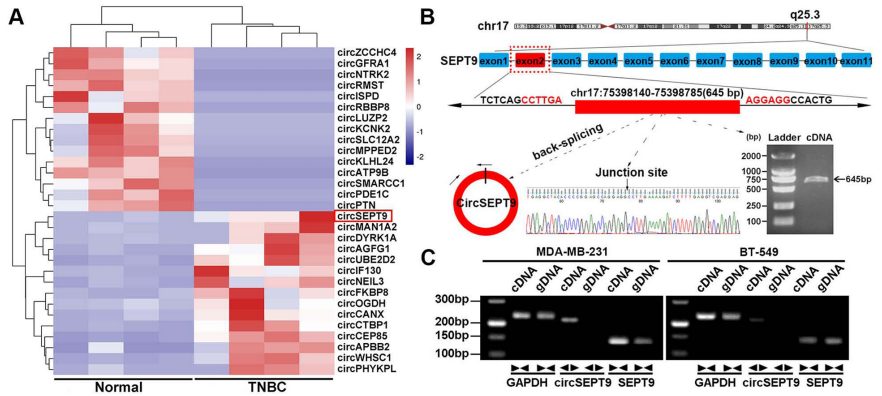
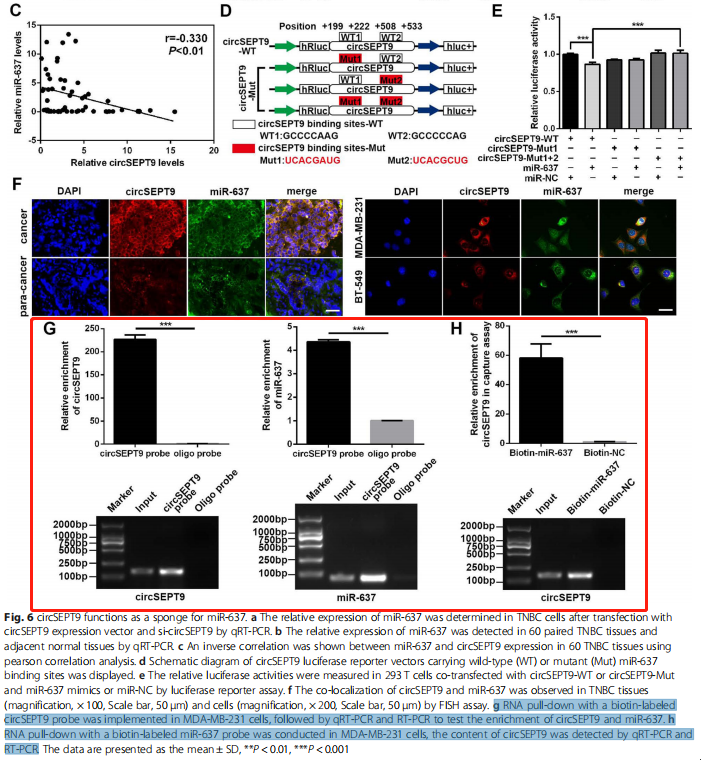
越來越多的研究表明,環(huán)狀RNA與許多癌癥的發(fā)生和發(fā)展密切相關(guān)。本研究旨在探討環(huán)狀RNA circSEPT9在人三陰乳腺癌(triple-negative breast cancer, TNBC)中的表達、生物學功能及分子機制,并分析其表達調(diào)控機制,為其作為TNBC臨床診斷和治療新的分子靶點提供科學依據(jù)。通過轉(zhuǎn)錄組測序(RNA sequencing, RNA-seq)分析4對TNBC組織和癌旁正常組織,得到差異表達的circRNA表達譜。采用Sanger測序、PCR擴增、RNA酶R消化及放線菌素D處理等方法鑒定circSEPT9。應用實時熒光定量PCR和原位雜交技術(shù)檢測TNBC患者中circSEPT9的表達,分析其表達與臨床病理特征的關(guān)系,進一步評價其預后。通過一系列體內(nèi)外功能實驗,包括染色質(zhì)免疫沉淀(ChIP)、熒光素酶報告基因和RIP分析、RNA pull down等,探討circSEPT9在TNBC發(fā)生發(fā)展中的作用及機制。本研究發(fā)現(xiàn)E2F1和EIF4A3可能促進circSEPT9的生物發(fā)生;證實了 E2F1和EIF4A3介導的circSEPT9能夠與miR-637結(jié)合促進LIF的表達及激活LIF/Stat3信號通路,進而促進三陰性乳腺癌的發(fā)生發(fā)展。因此,circSEPT9可作為TNBC潛在的生物標志物和治療靶點。

案例二
circPVT1可被HuR調(diào)控,通過miR-30d/e-CCNF通路促進肺鱗癌細胞的增殖

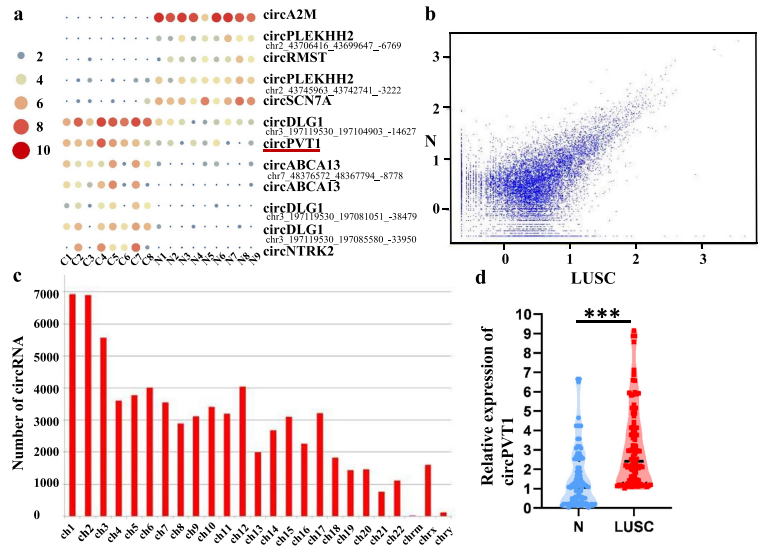
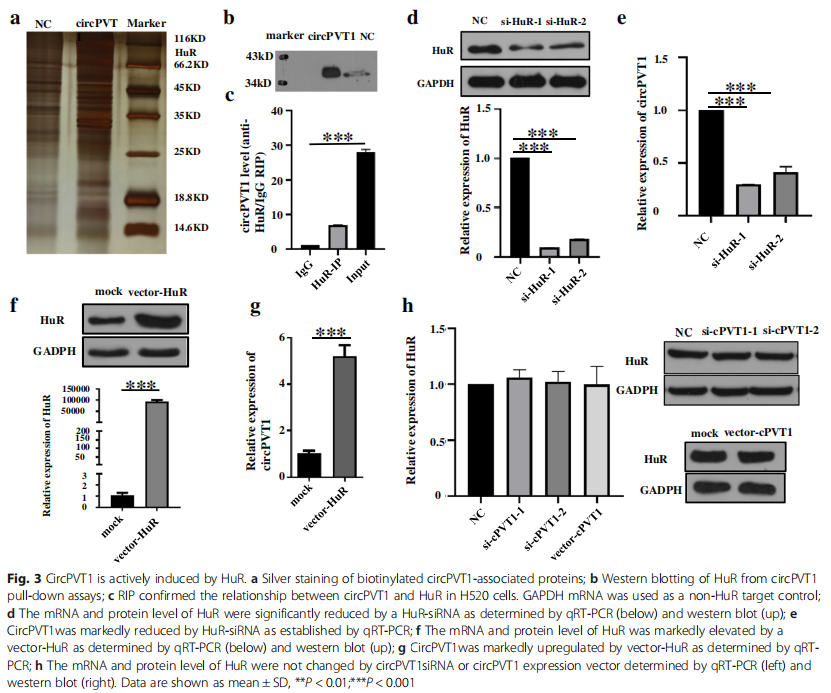
環(huán)狀RNA(circRNAs)是一類新型的廣泛存在的非編碼RNA,可以調(diào)控不同的人類疾病,包括癌癥的發(fā)生發(fā)展。然而,關(guān)于circRNAs在肺鱗狀細胞癌(LUSC)中的潛在機制和臨床意義的信息還很少。本研究使用RNA測序(RNA-seq)技術(shù)對LUSC組織和健康肺組織中的RNA表達譜進行了分析。qRT-PCR用于分析circPVT1的表達及其與LUSC預后(即生存分析)的關(guān)系,并進行了體外和體內(nèi)實驗以評估circPVT1對腫瘤生長的影響。作者運用RNA pull-down實驗、質(zhì)譜分析、雙熒光素酶報告基因分析和RNA免疫沉淀實驗,以探究circPVT1、HuR、miR-30d/e在LUSC中的相互作用。結(jié)果顯示circPVT1促進LUSC細胞的增殖。circPVT1可被HuR調(diào)控,circPVT1作為miR-30d和miR-30e的競爭性內(nèi)源性RNA(ceRNA),在減輕miR-30d和miR-30e對其靶基因CCNF的抑制影響方面發(fā)揮作用。綜上所述,circPVT1通過HuR/circPVT1/miR-30d和miR-30e/CCNF級聯(lián)通路促進LUSC進展,這使它有望成為LUSC診斷的新型生物標志物或治療靶點。

案例三
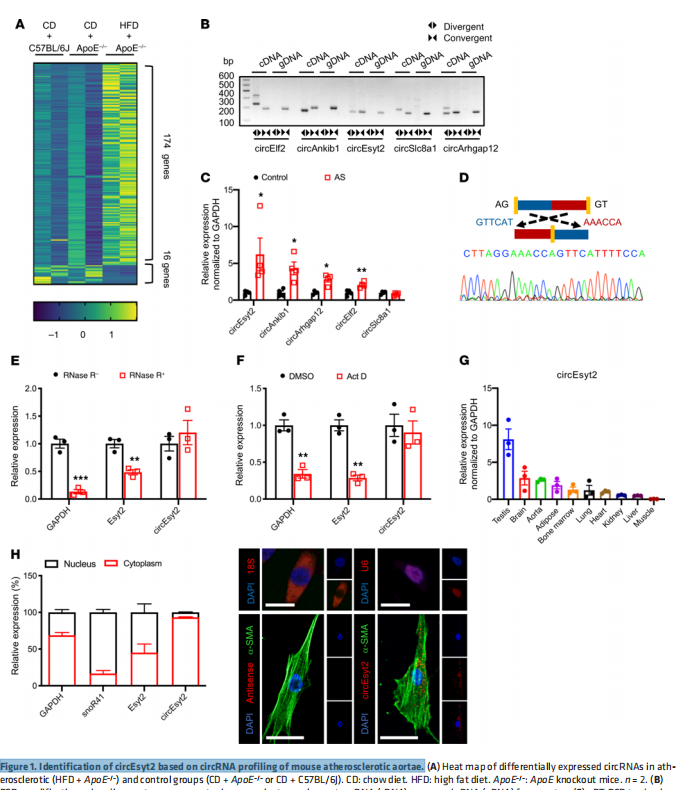
circEsyt2通過剪接調(diào)控來調(diào)節(jié)血管平滑肌細胞重構(gòu)

冠心病、腦卒中是病人致死、致殘的主要原因。然而,其發(fā)病機制不完全清楚,臨床仍需有效治療策略。因此,進一步揭示這些疾病發(fā)病機制顯得尤為重要。血管平滑肌細胞(VSMC)的表型轉(zhuǎn)化是冠心病、腦卒中、高血壓等重大心腦血管疾病發(fā)生發(fā)展的病理生理學基礎,如何抑制VSMC從收縮態(tài)向分泌態(tài)轉(zhuǎn)化成為大家共同關(guān)注的科學問題。
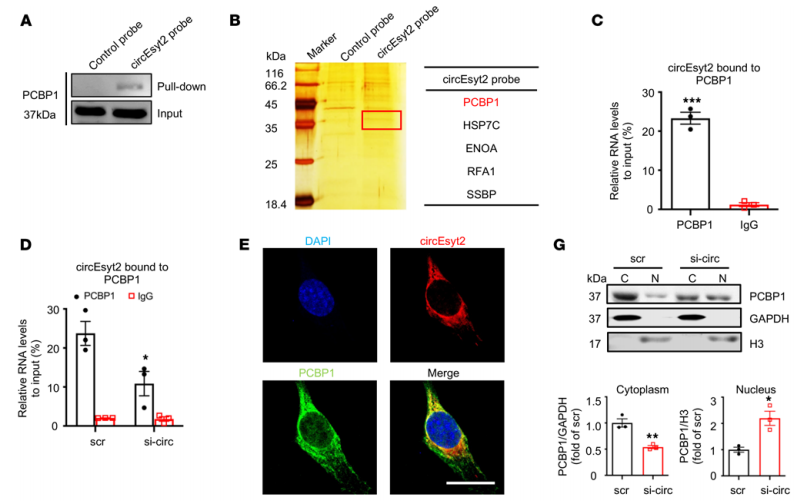
作者從多種VSMC表型轉(zhuǎn)化疾病小鼠模型中篩選出高表達環(huán)狀RNA-circEsyt2,通過表型研究發(fā)現(xiàn),circEsyt2可促進血管平滑肌細胞增殖、遷移和表型轉(zhuǎn)換等細胞行為。而在小鼠頸動脈損傷模型中,抑制circEsyt2表達可顯著減輕損傷后血管的內(nèi)膜新生,表明circEsyt2具有促進血管重塑的病理生理學功能。進一步研究發(fā)現(xiàn),位于細胞質(zhì)中的circEsyt2可以直接“吸附”剪接調(diào)控因子PCBP1并阻礙其入核,在核內(nèi)觸發(fā)p53基因的可變剪接事件,生成p53β,進而發(fā)揮調(diào)控血管平滑肌表型轉(zhuǎn)換及血管重構(gòu)的作用。此外,嚴重狹窄的患者冠脈平滑肌細胞中circEsyt2表達顯著升高,進一步提示其與疾病的密切關(guān)聯(lián)。該研究為血管重構(gòu)性疾病的防治新策略提供理論基礎和潛在靶點。


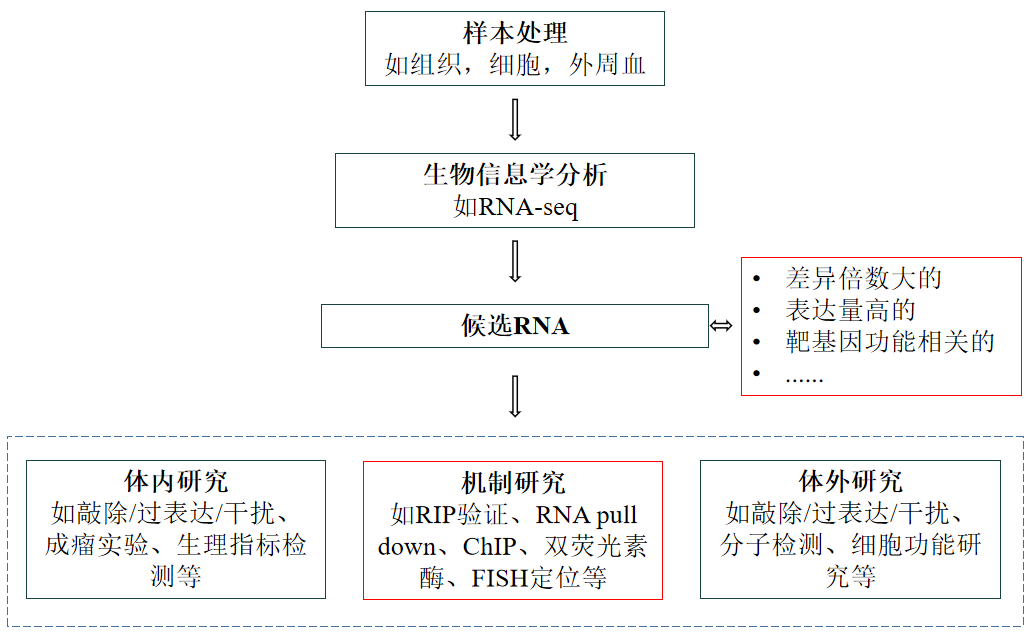
在探討了三個非編碼文獻案例后,我們可以總結(jié)出RNA功能研究的常規(guī)方案設計,并通過以下流程圖來直觀地表示:
武漢金開瑞生物工程有限公司作為一家專業(yè)致力于為全球制藥企業(yè)、診斷試劑企業(yè)、科研試劑研發(fā)企業(yè)、高校和科研院所以及大型醫(yī)院提供蛋白及核酸相關(guān)研究技術(shù)服務的高新技術(shù)企業(yè)。我們的服務內(nèi)容完善、項目經(jīng)驗豐富,涵蓋載體構(gòu)建、siRNA合成、細胞功能實驗,以及包括RNA pull down、RIP、ChIP等在內(nèi)的十余項分子互作技術(shù)及試劑盒產(chǎn)品。無論是基礎研究還是藥物開發(fā),金開瑞生物都是您值得信賴的合作伙伴,期待與您攜手共進,共同開啟RNA研究的探索之旅~
參考來源:
● https://www.cqmu.edu.cn/info/1096/4459.htm
● https://doi.org/10.1186/s13046-021-01976-w
● https://www.nsfc.gov.cn/publish/portal0/tab448/info82723.htm
● https://www.researchgate.net/publication/357060325
●https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-020-01183-9
最新動態(tài)
-
09.23
中藥的現(xiàn)代詮釋:外泌體如何革新傳統(tǒng)醫(yī)學?
-
07.02
1+1>2!深度解析RNA測序數(shù)據(jù)挖掘邏輯和后期實驗設計思路,輕松研獲10+ SCI
-
07.01
“稻”亦有道——盤點近期水稻研究的重大突破
-
06.28
科學與美學的結(jié)合體:植物亞細胞定位技術(shù)詳解
-
06.28
“聚焦新質(zhì)生產(chǎn)力,激發(fā)科研新動能”|LCA躋身蛋白互作研究的新銳力量
-
06.05
知無不“研”|一文讀懂免疫共沉淀技術(shù)(Co-IP)
-
05.14
四大研究利器(Co-IP、BIFC、Y2H、GST pull-down)助力速配蛋白互作“最佳拍檔”
-
05.14
高效、精準、直觀、實時——取經(jīng)“蛋白互作研究翹楚”BIFC!
-
05.14
轉(zhuǎn)染效率低、干擾效果差、重復性欠佳...siRNA研究頻遇“攔路虎”怎么辦?
-
04.22
一文讀懂EMSA技術(shù)核心要點,讓“emsa” 秒變“easy”










