RNA pull down—研究RNA與蛋白互作的法寶
信息來源:金開瑞 作者:genecreate 發(fā)布時(shí)間:2018-05-10 14:35:15
RNA與蛋白質(zhì)的相互作用是細(xì)胞生理過程得以實(shí)現(xiàn)的決定性因素之一。近年來,隨著技術(shù)的改進(jìn)和新方法的建立,RNA和蛋白質(zhì)的相互作用研究取得了長足進(jìn)步。目前科研人員已經(jīng)鑒定了較多RNA上的蛋白質(zhì)結(jié)合位點(diǎn),也發(fā)現(xiàn)了許多蛋白質(zhì)中的RNA結(jié)合結(jié)構(gòu)域,并對它們的結(jié)構(gòu)特征進(jìn)行了比較詳細(xì)的研究。這些為最終探明RNA和蛋白質(zhì)相互作用的分子機(jī)制,從而從本質(zhì)上認(rèn)識相關(guān)的細(xì)胞生理過程打下了堅(jiān)實(shí)的基礎(chǔ)。
RNA pull-down作為研究RNA與蛋白互作的核心技術(shù),已成為研究焦點(diǎn)。RNA pull down是使用體外轉(zhuǎn)錄法標(biāo)記生物素RNA探針,然后與胞漿蛋白提取液孵育,形成RNA-蛋白質(zhì)復(fù)合物。該復(fù)合物可與鏈霉親和素標(biāo)記的磁珠結(jié)合,從而與孵育液中的其他成分分離。復(fù)合物洗脫后,通過WB實(shí)驗(yàn)檢測特定的RNA結(jié)合蛋白是否與RNA相互作用,或者結(jié)合MS篩選RNA結(jié)合的未知蛋白。
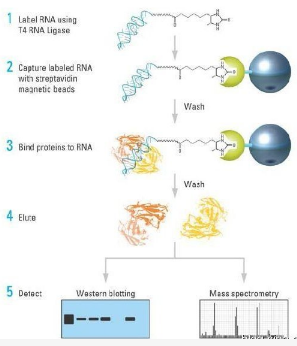
RNA pull down技術(shù)應(yīng)用
1.癌癥腫瘤相關(guān)調(diào)控機(jī)制研究
LncRNA發(fā)揮功能的方式很廣,可以與蛋白、DNA和RNA相互作用,參與多種生物學(xué)過程的調(diào)控。主要包括基因組表觀遺傳修飾、調(diào)控轉(zhuǎn)錄后翻譯、發(fā)揮ceRNA、增強(qiáng)子RNA作用等,從而對細(xì)胞的增殖、分化、遷移、凋亡、免疫等發(fā)揮調(diào)控作用。
lncRNA能夠通過對腫瘤細(xì)胞糖代謝、谷氨酰胺代謝和脂類代謝途徑中的關(guān)鍵環(huán)節(jié)進(jìn)行調(diào)節(jié),導(dǎo)致腫瘤細(xì)胞對葡萄糖攝取增加、谷氨酰胺分解增強(qiáng)及脂質(zhì)生成增加,從而促進(jìn)腫瘤的發(fā)生和發(fā)展。目前,大多數(shù)lncRNA在腫瘤細(xì)胞能量代謝中的功能和調(diào)控機(jī)制尚不完全清楚,進(jìn)一步認(rèn)識和了解腫瘤細(xì)胞中與lncRNA相關(guān)的能量代謝異常表現(xiàn)出的惡性生物學(xué)行為,將有助于為腫瘤的診斷和治療提供有效的證據(jù)及新的思路和途徑。
環(huán)狀RNA(circular RNA,circRNA)是近來研究很熱門的一種特殊的長鏈非編碼RNA。研究發(fā)現(xiàn),circRNA 在人體細(xì)胞中廣泛表達(dá),在轉(zhuǎn)錄后水平具有調(diào)控基因表達(dá)的重要功能,并且參與多種腫瘤和其他疾病的病理發(fā)展過程
circRNA大多由外顯子序列組成,呈閉合環(huán)狀結(jié)構(gòu),性質(zhì)穩(wěn)定,高度保守性,通過微小RNA“海綿”作用調(diào)控靶基因表達(dá),與腫瘤的發(fā)生、發(fā)展相關(guān)。這些特性使circRNA有潛力成為腫瘤新型分子診斷標(biāo)志物。通過競爭性與腫瘤相關(guān)微小RNA的結(jié)合,可以開發(fā)針對circRNA分子靶點(diǎn)的靶向治療藥。因此,circRNA在腫瘤轉(zhuǎn)化醫(yī)學(xué)研究中意義巨大。
2.多種人類疾病研究
RBPs在轉(zhuǎn)錄后水平參與調(diào)控mRNA穩(wěn)定性、LncRNA活性、應(yīng)激、腫瘤發(fā)生發(fā)展、細(xì)胞凋亡等眾多生物學(xué)過程,且與諸多人類疾病密切相關(guān)。因此,對RBPs-RNAs相互作用網(wǎng)絡(luò)的研究和鑒定有重要意義。但由于RBPs作用方式復(fù)雜、功能多樣性、作用空間位置多樣化等原因,對其開展精確研究一直是一個(gè)重大挑戰(zhàn)。RNA領(lǐng)域,尤其是非編碼RNA研究的快速發(fā)展,催生了多種RBPs-RNAs相互作用鑒定技術(shù)。
| 問題 | 原因 | 解決方案 |
| RNA結(jié)合蛋白的親和力不夠 |
1)結(jié)合緩沖環(huán)境沒有優(yōu)化 2)裂解不完全 3)磁珠用量不足 4)RNA探針用量不足 |
1)優(yōu)化孵育時(shí)間、溫度 、鹽濃度等條件 2)增加裂解液和蛋白上樣量的比例 3)增加裂解液 4)增加磁珠或探針用量 5)確定生物素和鏈霉親和素效率 |
| RNA結(jié)合蛋白沒有結(jié)合 |
1)靶蛋白量不足 2)緩沖體系不對 3)RNA探針和蛋白的親和力本來就低 |
1)增加上樣蛋白量 2)應(yīng)用低鹽體系 3)加入交聯(lián)試劑 |
| WB信噪比高 |
1)陽性信號率低 2)一抗效率低 3)蛋白沒有充分溶解 |
1)增加二抗的量 2)用敏感度的化學(xué)發(fā)光液 3)用細(xì)胞裂解液預(yù)孵一抗 4)增加樣品的量 5)確定有沒有其他可能的結(jié)合情況 6)增加裂解液用量 |
| 結(jié)合的非特異性高 |
1)緩沖環(huán)境沒有優(yōu)化 2)緩沖環(huán)境嚴(yán)謹(jǐn)性低 3)樣品沒有裂解完全和裂解體系沒有優(yōu)化 |
1)優(yōu)化孵育時(shí)間溫度 鹽濃度等條件 2)使用嚴(yán)謹(jǐn)性高的緩沖體系 3)調(diào)低RNA探針和樣品的比例 4)提高裂解液的量 |
案例展示
案例一
題目:The STAT3-Binding Long Noncoding RNA lnc-DC Controls Human Dendritic Cell Differentiation
小結(jié):RNA pull-down設(shè)置實(shí)驗(yàn)組及反義鏈對照組,銀染找出差異條帶進(jìn)行膠條質(zhì)譜鑒定,分析結(jié)果篩選得到STAT3蛋白,進(jìn)一步通過RIP-qPCR反向驗(yàn)證,證實(shí)STAT3蛋白可以與lnc-DC結(jié)合。
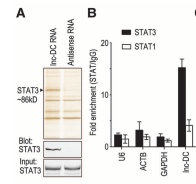
Lnc-DC pull-down銀染檢測及RIP驗(yàn)證Lnc-DC與STAT3互作
案例二
題目:The long noncoding RNA THRIL regulates TNFα expression through its interaction with hnRNPL
小結(jié):先用Linc1992全長進(jìn)行RNA pull-down實(shí)驗(yàn),通過WB檢測手段分析四個(gè)意向蛋白中篩選得到一個(gè)差異蛋白α-hnRNPL,通過分段RNA pull-down及WB分析核心結(jié)合區(qū)域,主要是Linc1992的1-699和1406-2012區(qū)域,通過RIP-qPCR反向驗(yàn)證,證明α-hnRNPL蛋白可以與Linc1992結(jié)合。
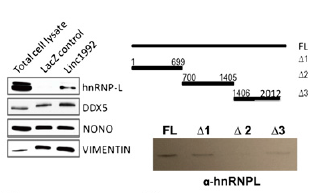
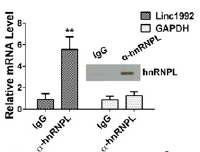
Linc1992 pull down-WB篩選差異蛋白同時(shí)結(jié)合RIP驗(yàn)證Linc1992與α-hnRNPL互作
最新動態(tài)
-
09.23
中藥的現(xiàn)代詮釋:外泌體如何革新傳統(tǒng)醫(yī)學(xué)?
-
07.02
1+1>2!深度解析RNA測序數(shù)據(jù)挖掘邏輯和后期實(shí)驗(yàn)設(shè)計(jì)思路,輕松研獲10+ SCI
-
07.01
“稻”亦有道——盤點(diǎn)近期水稻研究的重大突破
-
06.28
科學(xué)與美學(xué)的結(jié)合體:植物亞細(xì)胞定位技術(shù)詳解
-
06.28
“聚焦新質(zhì)生產(chǎn)力,激發(fā)科研新動能”|LCA躋身蛋白互作研究的新銳力量
-
06.05
知無不“研”|一文讀懂免疫共沉淀技術(shù)(Co-IP)
-
05.14
四大研究利器(Co-IP、BIFC、Y2H、GST pull-down)助力速配蛋白互作“最佳拍檔”
-
05.14
高效、精準(zhǔn)、直觀、實(shí)時(shí)——取經(jīng)“蛋白互作研究翹楚”BIFC!
-
05.14
轉(zhuǎn)染效率低、干擾效果差、重復(fù)性欠佳...siRNA研究頻遇“攔路虎”怎么辦?
-
04.22
一文讀懂EMSA技術(shù)核心要點(diǎn),讓“emsa” 秒變“easy”
找回密碼
注冊帳號
-
 在線客服
在線客服 -

 在線訂購
在線訂購 -

 掃碼領(lǐng)資料
掃碼領(lǐng)資料掃碼領(lǐng)資料

電話:19522948401
-

 文獻(xiàn)獎(jiǎng)勵(lì)申請
文獻(xiàn)獎(jiǎng)勵(lì)申請


