siRNA介紹及藥物研發的現狀前景
RNA(核糖核酸)作為細胞內的重要分子之一,在生物學和醫學領域中扮演著不可替代的角色。其功能不僅限于傳遞遺傳信息,還涉及到基因表達調控、蛋白質合成等多個生物學過程。近年來,RNA干擾技術的發展為研究人員提供了一種強大的工具,尤其是siRNA(小干擾RNA),其引人注目的特性使其成為基因沉默和藥物研發領域的熱門話題。
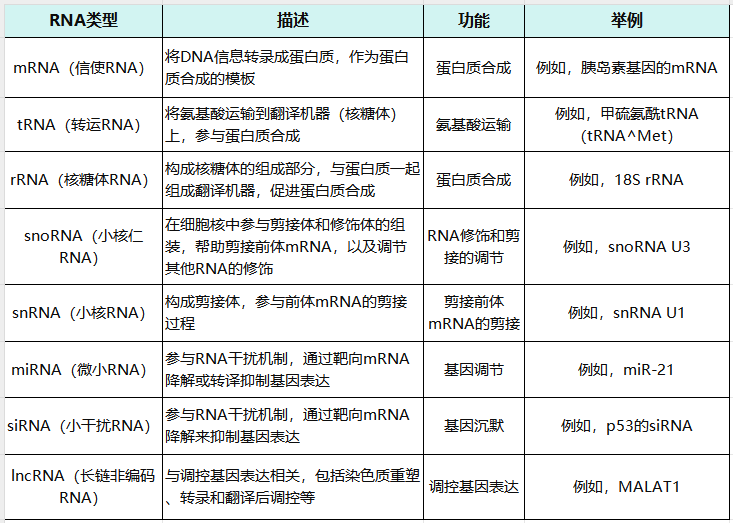
圖1. RNA類型及其特點歸納
siRNA的發現和研究歷程堪稱令人矚目。1998年,安德魯·法爾等科學家發現了RNA干擾(RNAi)現象,這是一種在真核細胞中自然存在的機制,可以特異性地降解目標mRNA從而抑制基因的表達。2001年,托馬斯·蒂什等人證明了siRNA可以在哺乳動物細胞中有效誘導RNAi。他們展示了合成的短雙鏈RNA可以被細胞內的RNAi機制識別并用來沉默特定的基因。2006年,安德魯·法爾和克雷格·梅洛因為他們在RNA干擾方面的開創性工作共同獲得了諾貝爾生理學或醫學獎。至此之后,大型制藥公司已經投入了數十億美元用于人類基因沉默治療的開發。
2018年8月標志著RNA干擾治療的新紀元,FDA批準了首個基于siRNA技術的藥物——Patisiran(商品名ONPATTRO™),用于治療遺傳性轉甲狀腺素淀粉樣變性(hATTR)引起的神經損傷。近年來,siRNA技術繼續在多個領域展現出巨大的潛力,包括作為治療各種遺傳性疾病、病毒感染和癌癥的潛在藥物,以及在基礎生物學研究中用于基因功能分析。
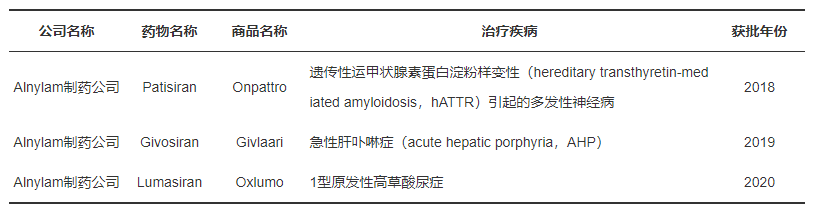
圖2. FDA批準上市的siRNA藥物
(圖源:10.16476/j.pibb.2021.0102)
對于藥物開發人員而言,siRNA療法的潛力是不容忽視的。傳統藥物治療的效果常常受到藥物代謝障礙和不完全吸收的限制,導致藥物生物利用度降低。此外,藥物對健康細胞的反向作用也可能帶來一系列副作用。相比之下,基因治療作為一種前沿的治療策略,能夠在基因層面從根本上解決疾病問題,為治療提供了更多的可能性和靈活性。通過精確識別特定疾病的致病基因,研究人員可以設計特定的siRNA來靶向這些基因的mRNA,并裂解它們,以達到治療疾病的目的。siRNA的分子治療因其在治療各種癌癥、病毒感染、遺傳性疾病和疼痛管理等方面的巨大潛力而備受關注,并且有望為許多目前尚無有效治療方法的疾病找到新的解決方案,為人類健康帶來更大的福祉。
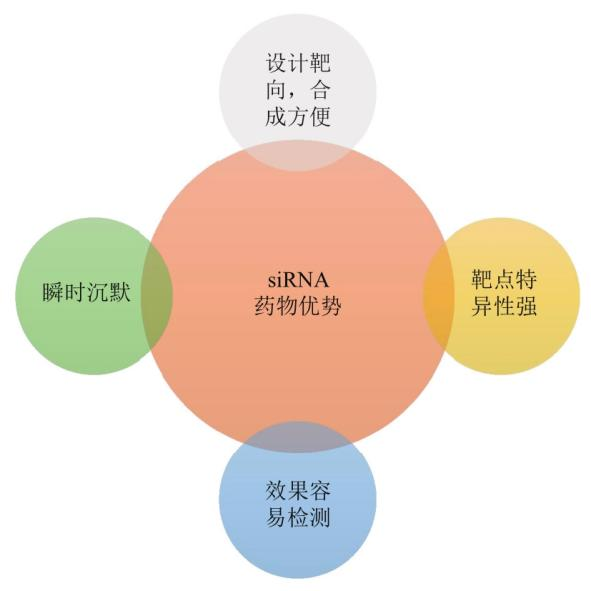
圖3. siRNA藥物的優勢
(圖源:10.16476/j.pibb.2021.0102)
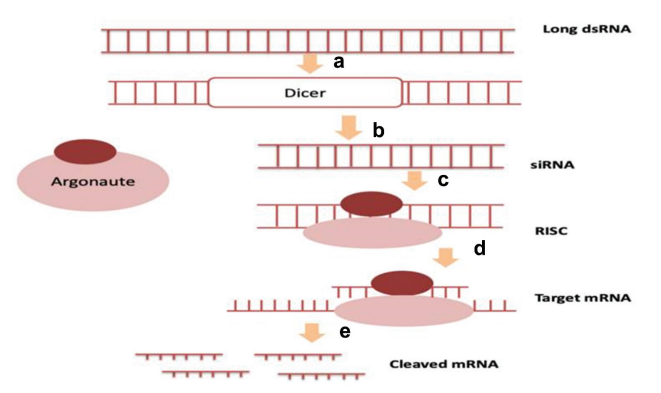
圖4. mRNA(基因)通過siRNA途徑沉默
(圖源:10.1080/17425247.2023.2251890)
siRNA藥物臨床開發的進步,促進了siRNA藥物開發過程的日益成熟。但其中遇到的許多挫折,也使藥物開發過程更加復雜。siRNA作為藥物存在半衰期短、血漿穩定性差、易被核酸酶降解,且siRNA帶負電荷不易透過帶負電荷的細胞膜進入腫瘤細胞,容易被細胞內的溶酶體降解等諸多挑戰。
因此,siRNA作為藥物很難直接用于疾病治療,需要采取一定的手段實現其在生物體內的有效遞送并達到治療疾病的目的。其中,利用納米載體構建siRNA藥物納米遞送系統進行siRNA藥物的遞送是實現siRNA藥物進行治療時的常用手段。目前納米載體用來包載的基因主要包括:DNA、RNA(siRNA)、反義寡核苷酸藥物(antisense oligodeoxynucleotides,AODNs)和microRNA等。
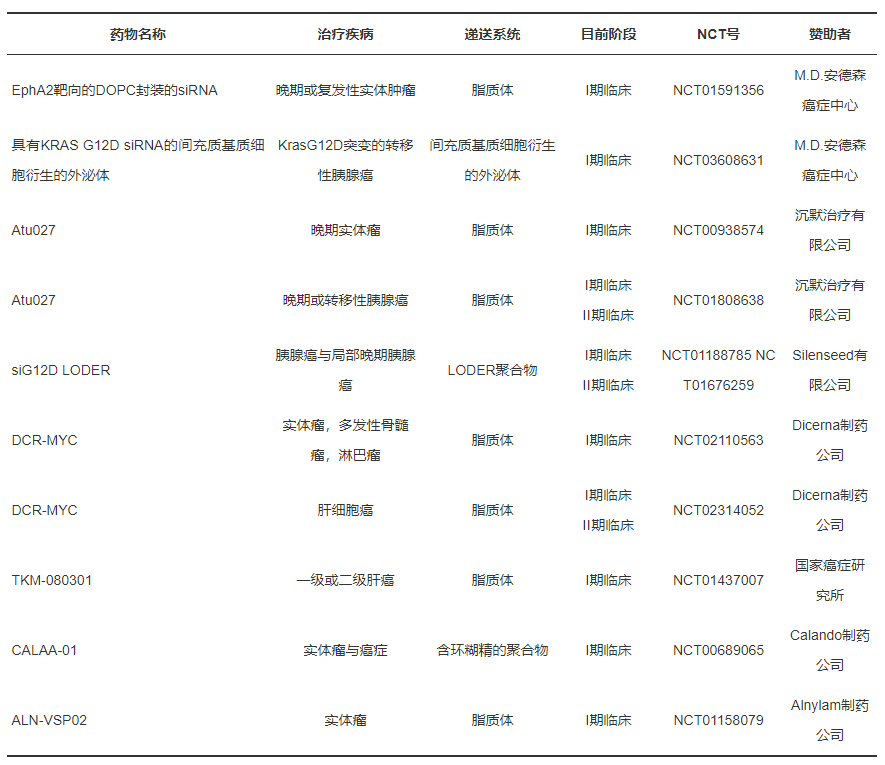
圖5. 臨床試驗中的siRNA納米遞送系統
(圖源:10.16476/j.pibb.2021.0102)
未來,隨著更多研究的開展和技術的突破,siRNA的應用前景將更加廣闊。回歸根本,在進行基因功能研究、藥物篩選或疾病治療研究時,高品質的siRNA是不可或缺的關鍵工具。武漢金開瑞生物工程有限公司,作為專注于為全球制藥、診斷試劑及科研試劑研發企業、高校和科研院所以及大型醫院提供高質量蛋白及相關研究技術服務的高新技術企業,致力于為客戶提供前沿的核酸和蛋白研究策略。
在這春暖花開的陽春三月,金開瑞生物特推出“siRNA狂歡購系列活動”,旨在以極具吸引力的折扣價格向廣大科研工作者及醫藥專業人士提供優質的siRNA產品。我們期待與全球的合作伙伴攜手共進,深入挖掘siRNA在生命科學領域的無限潛能,為人類健康事業作出更加卓越的貢獻。詳詢即享優惠~
參考文獻:
[1]Fire, A., Xu, S., Montgomery, M. K., Kostas, S. A., Driver, S. E., & Mello, C. C. (1998). Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans. Nature, 391(6669), 806-811.
[2]Elbashir, S. M., Harborth, J., Lendeckel, W., Yalcin, A., Weber, K., & Tuschl, T. (2001). Duplexes of 21-nucleotide RNAs mediate RNA interference in cultured mammalian cells. Nature, 411(6836), 494-498.
[3]Mello, C. C., & Conte Jr, D. (2004). Revealing the world of RNA interference. Nature, 431(7006), 338-342.
[4]Whitehead, K. A., Langer, R., & Anderson, D. G. (2009). Knocking down barriers: advances in siRNA delivery. Nature Reviews Drug Discovery, 8(2), 129-138.
[5]Burnett, J. C., Rossi, J. J., & Tiemann, K. (2011). Current progress of siRNA/shRNA therapeutics in clinical trials. Biotechnology Journal, 6(9), 1130-1146.
[6]10.16476/j.pibb.2021.0102
[7]https://doi.org/10.3390/ijms24043375
[8]10.1080/17425247.2023.2251890
[9]http://www.rnajournal.org/cgi/doi/10.1261/rna.5103703
最新動態
-
09.23
中藥的現代詮釋:外泌體如何革新傳統醫學?
-
07.02
1+1>2!深度解析RNA測序數據挖掘邏輯和后期實驗設計思路,輕松研獲10+ SCI
-
07.01
“稻”亦有道——盤點近期水稻研究的重大突破
-
06.28
科學與美學的結合體:植物亞細胞定位技術詳解
-
06.28
“聚焦新質生產力,激發科研新動能”|LCA躋身蛋白互作研究的新銳力量
-
06.05
知無不“研”|一文讀懂免疫共沉淀技術(Co-IP)
-
05.14
四大研究利器(Co-IP、BIFC、Y2H、GST pull-down)助力速配蛋白互作“最佳拍檔”
-
05.14
高效、精準、直觀、實時——取經“蛋白互作研究翹楚”BIFC!
-
05.14
轉染效率低、干擾效果差、重復性欠佳...siRNA研究頻遇“攔路虎”怎么辦?
-
04.22
一文讀懂EMSA技術核心要點,讓“emsa” 秒變“easy”










