蛋白質(zhì)組學(xué)揭示AHLs誘導(dǎo)Geobacter soli生物膜形成和電活性機(jī)制
信息來源:金開瑞 作者:genecreate 發(fā)布時間:2019-01-10 17:09:38
題目:Chemical signals stimulate Geobacter soli biofilm formation and electroactivity
蛋白質(zhì)組學(xué)揭示AHLs誘導(dǎo)Geobacter soli生物膜形成和電活性機(jī)制
期刊:Biosensors and Bioelectronic
影響因子:8.173
合作技術(shù):SWATH
研究背景
生物膜在污水處理系統(tǒng)中被廣泛應(yīng)用,其中電化學(xué)生物膜(Electroactive biofilms, EABs)因具有向固體材料(如電極)傳遞電子的能力,是廢水處理和其他污染控制措施中最有前途的生物膜類型之一,同時EABs的形成和調(diào)控對生物電化學(xué)系統(tǒng)(BES)性能至關(guān)重要。已有研究證明群體感應(yīng)(Quorum sensing, QS)系統(tǒng)對BESs中EABs性能產(chǎn)生影響,N-酰基高絲氨酸內(nèi)酯(AHLs)是細(xì)菌調(diào)節(jié)群體感應(yīng)的通信因子。目前Geobacter sp.的電化學(xué)活性和生物膜的形成是否受到AHLs的影響,以及Geobacter sp.是否產(chǎn)生內(nèi)源性AHLs尚未見報道。
研究內(nèi)容及結(jié)果
1. AHLs促進(jìn) Geobacter soli生物膜形成和電化學(xué)活性
作者分別用兩種外源AHLs,包括C6-HSL和3OC12-HSL,處理 Geobacter soli,發(fā)現(xiàn)和對照組相比,含外源AHLs的EABs與陽極相關(guān)的生物量最多,而不含AHLs的EABs生物量明顯較少。激光共聚焦激光掃描顯微鏡(CLSM)圖像揭示了內(nèi)源性和外源性AHLs對生物膜形成的積極作用。利用外源性AHLs的實(shí)驗組觀察到圖1中可見的成熟生物膜,同樣,添加酰基酶后,其生物量和生物膜形成均低于對照組,說明G. soli分泌的內(nèi)源性AHLs和外源性AHLs具有相同的功能。
作者發(fā)現(xiàn)在AHLs存在下,BESs的啟動時間縮短,電流輸出增強(qiáng)(圖2a)。具有外源性AHLs和內(nèi)源性AHLs的BESs在第4天開始出現(xiàn)明顯的電流峰值,只有內(nèi)源性AHLs的BESs和沒有內(nèi)源性AHLs的BESs分別在第12天和第20天達(dá)到初始電流峰值。為了證實(shí)酰基酶的AHLs降解功能,作者進(jìn)行了AHLs和酰基酶同時存在的處理組。以上實(shí)驗結(jié)果表明,外源性和內(nèi)源性AHLs在BESs中發(fā)揮調(diào)節(jié)作用。
隨后,作者采用CV法研究AHLs對G. soli 的EABs氧化還原活性的影響。結(jié)果顯示,外源性AHLs的G. soli EABs在所有處理中催化電流最高(圖2b)。而在無菌PBS中加入AHLs和酰基酶未見氧化還原峰,這說明所有氧化還原信號均由生物膜基氧化還原化合物引起。EABs的電化學(xué)阻抗譜(EIS)用于反映細(xì)胞外電子轉(zhuǎn)移過程,該過程涉及以電流輸出測量的總體電子轉(zhuǎn)移速率。在無內(nèi)源性和外源性AHLs時,BESs的Rct和Rbiofilm均最高(圖2c)。相比之下,外源性AHLs處理的電荷轉(zhuǎn)移電阻(Rct)值和生物膜電阻(Rbiofilm)值最低,這說明AHLs能有效提高G. soli EABs的電荷轉(zhuǎn)移能力和電導(dǎo)率。
受電子能力(EAC)和供電子能力(EDC)可用于表征胞外聚合物(EPS)中電化學(xué)活性物質(zhì)如外膜細(xì)胞色素C的電活性。如圖3所示,無內(nèi)源性AHLs的總EPS的EAC略低于對照組。添加C6-HSL的EPS總EDC和EAC分別比對照組高75%和50%,添加3OC12-HSL的EPS總EDC比對照組高50%,說明外源性AHLs可增強(qiáng)EPS的氧化還原活性。綜上所述,結(jié)果表明內(nèi)源性和外源性AHLs均能提高G. soli EABs的電化學(xué)活性。
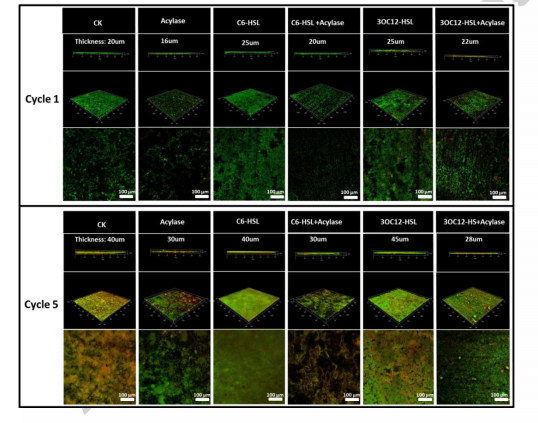
圖1 CLSM結(jié)果
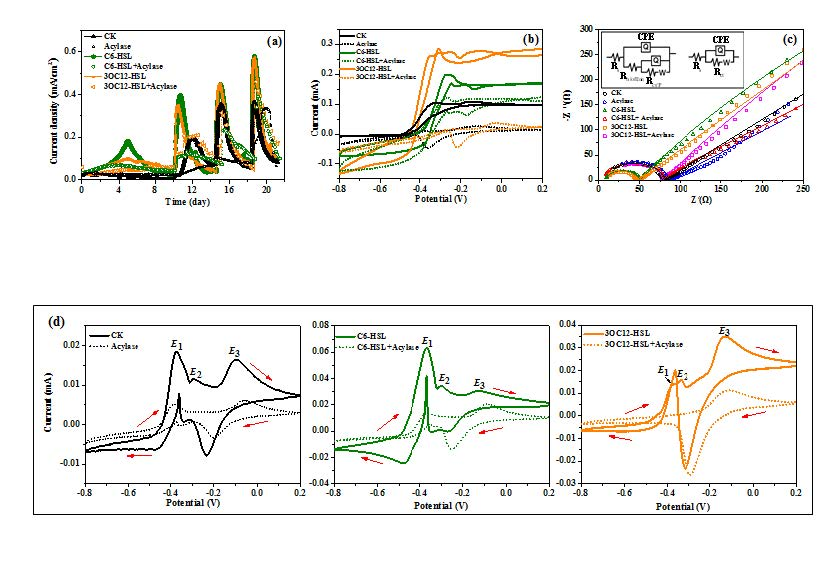
圖2 EABs電化學(xué)性能
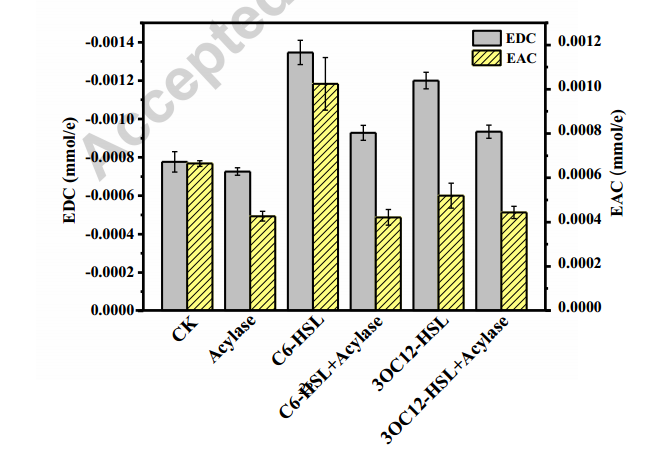
圖3 EPS的EAC和EDC值
2. 外源性和內(nèi)源性AHLs均促進(jìn)膜表面蛋白形成
由于添加了酰基酶的實(shí)驗組生物膜的形成和電活性均低于對照組,因此,作者認(rèn)為G. soli可以分泌內(nèi)源性AHL,質(zhì)譜鑒定證明了這一點(diǎn)(圖4)。電化學(xué)原位FTIR光譜可以識別生物膜形成過程中參與細(xì)胞外電子傳遞通路的分子,從分子水平揭示了氧化還原對的電化學(xué)反應(yīng)。條帶隨電位變化與細(xì)胞電極界面氧化還原反應(yīng)有關(guān),結(jié)果表明內(nèi)源性AHLs可以提高外膜蛋白的相對豐度,外源性AHLs的加入能夠進(jìn)一步促進(jìn)G. soli生物膜中羰基與酰胺的形成,使與酰胺的氫鍵更強(qiáng)。
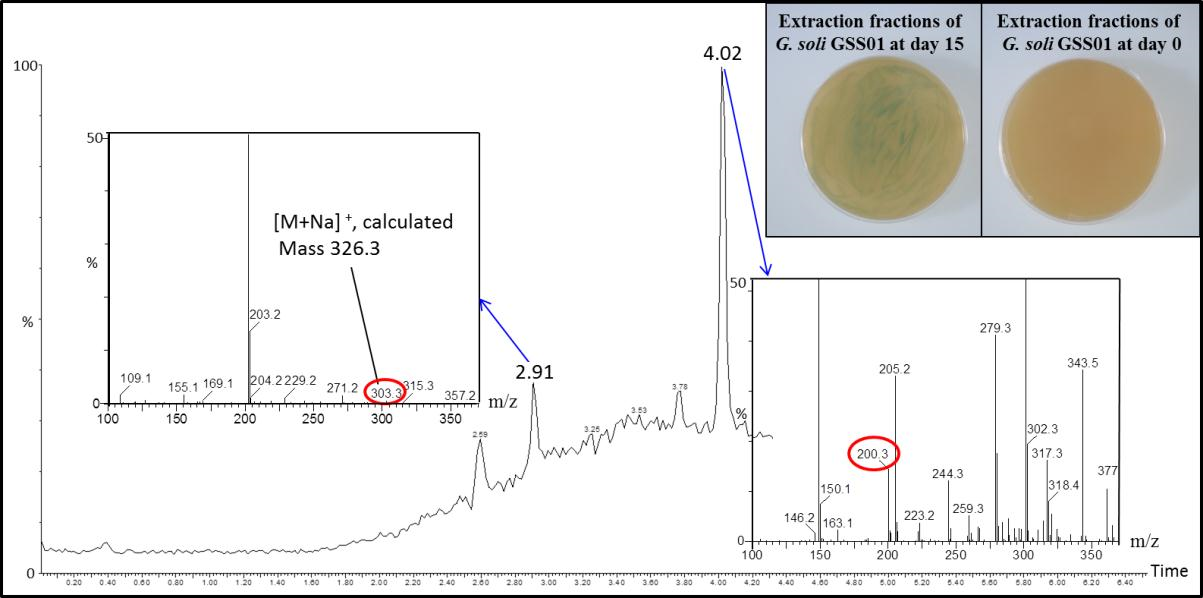
圖4 質(zhì)譜檢測內(nèi)源性AHLs
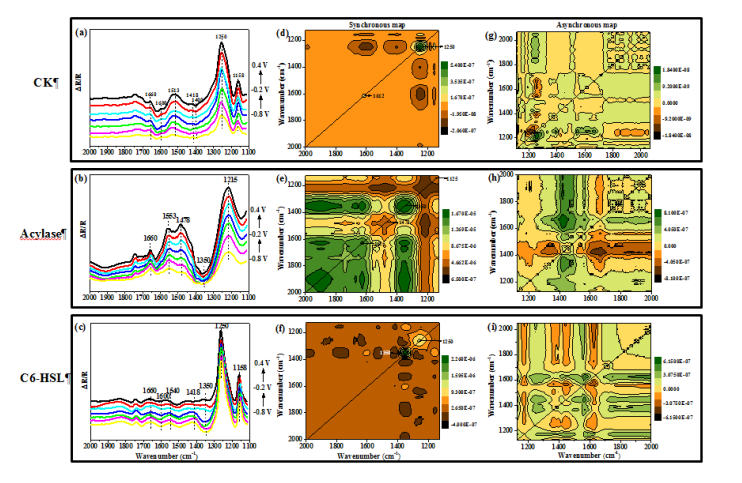
圖5 FTIR分析
3. 蛋白質(zhì)組學(xué)揭示AHLs作用機(jī)制
接下來,作者選用SWATH-MS定量蛋白質(zhì)組學(xué)技術(shù)研究單個細(xì)胞對AHLs反應(yīng)的多種機(jī)制。發(fā)現(xiàn)內(nèi)源性AHLs與外源性AHLs生物膜中分別有445和15個差異表達(dá)蛋白。COG功能注釋表明,暴露于酰基酶的生物膜下調(diào)蛋白多參與能量的產(chǎn)生與轉(zhuǎn)化、核苷酸的轉(zhuǎn)運(yùn)與代謝、碳水化合物的轉(zhuǎn)運(yùn)與代謝以及氨基酸的轉(zhuǎn)運(yùn)與代謝。內(nèi)源性AHLs可以影響上述過程中蛋白的表達(dá)水平,進(jìn)而影響生物膜的形成。參與EPS生產(chǎn)的關(guān)鍵酶包括磷酸烯醇丙酮酸合成酶、三磷酸異構(gòu)酶、葡萄糖-6-磷酸異構(gòu)酶以及磷酸葡聚糖酶,這些關(guān)鍵酶在AHLs存在下表達(dá)量均顯著上調(diào)。這說明內(nèi)源性AHLs可能促進(jìn)關(guān)鍵酶的表達(dá),提高EPS產(chǎn)量。此外,許多與代謝過程相關(guān)的蛋白,如在三羧酸(TCA)循環(huán)中起關(guān)鍵作用的檸檬酸合成酶,在沒有內(nèi)源性AHLs的情況下表達(dá)量下調(diào),說明內(nèi)源性AHLs也會影響G. soli的代謝活性。加外源性AHL后,與電子轉(zhuǎn)移相關(guān)的NADH脫氫酶表達(dá)量上調(diào)3倍,這可能是由于添加外源性AHL后電流密度較高。綜上,內(nèi)源性和外源性AHLs對G. soli生物膜的電活性均有明顯的正向影響,外源性AHLs對個體G. soli蛋白表達(dá)的進(jìn)一步影響,誘導(dǎo)了優(yōu)勢電流生成。
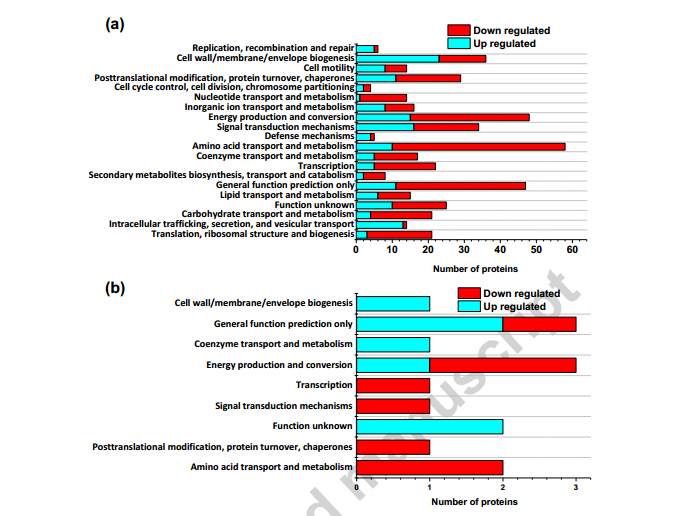
圖6 COG分析
文章小結(jié)
Geobacter soli GSS01可以分泌內(nèi)源性AHLs,提高外膜蛋白的相對豐度。內(nèi)源性AHLs通過促進(jìn)糖異生途徑的關(guān)鍵酶的表達(dá)影響EPS的形成。此外,內(nèi)源性AHLs在單個G. soli細(xì)胞的能量轉(zhuǎn)換、物質(zhì)轉(zhuǎn)運(yùn)和代謝等生理性能方面發(fā)揮著重要作用。外源AHLs進(jìn)一步促進(jìn)了G. soli生物膜中酰胺II的形成以及羰基與酰胺之間形成更強(qiáng)的氫鍵。本研究揭示了化學(xué)信號在Geobacter sp.體內(nèi)的重要性,為揭示內(nèi)源性和外源性AHLs的刺激機(jī)制提供了初步的科學(xué)依據(jù)。
解析文獻(xiàn)
Xianyue Jing, Xing Liu, et al. Chemical signals stimulate Geobacter soli biofilm formation and electroactivity[J]. Biosensors and Bioelectronic, 2018, 127:1-9.
相關(guān)服務(wù)
SWATH(Sequential Window Acquisition of all THeoretical Mass Spectra)是瑞士蘇黎世聯(lián)邦理工學(xué)院的Ruedi Aebersold 博士及其團(tuán)隊與SCIEX聯(lián)合推出的一項質(zhì)譜技術(shù)。SWATH采集模式將掃描范圍劃分為以25 Da為間隔的一系列區(qū)間,通過超高速掃描來獲得掃描范圍內(nèi)全部離子的所有碎片信息,是 MS/MS ALL技術(shù)的擴(kuò)展。SWATH技術(shù)是一種真正全景式的、高通量的質(zhì)譜技術(shù),同時也大大提高了定量的可重現(xiàn)性。
SWATH定量相比傳統(tǒng)的基于母離子強(qiáng)度的DDA定量有選擇性好、定量準(zhǔn)確等優(yōu)點(diǎn),適用于藥物作用靶點(diǎn)研究、疾病標(biāo)志物篩選、植物脅迫/抗逆研究等。
最新動態(tài)
-
09.23
中藥的現(xiàn)代詮釋:外泌體如何革新傳統(tǒng)醫(yī)學(xué)?
-
07.02
1+1>2!深度解析RNA測序數(shù)據(jù)挖掘邏輯和后期實(shí)驗設(shè)計思路,輕松研獲10+ SCI
-
07.01
“稻”亦有道——盤點(diǎn)近期水稻研究的重大突破
-
06.28
科學(xué)與美學(xué)的結(jié)合體:植物亞細(xì)胞定位技術(shù)詳解
-
06.28
“聚焦新質(zhì)生產(chǎn)力,激發(fā)科研新動能”|LCA躋身蛋白互作研究的新銳力量
-
06.05
知無不“研”|一文讀懂免疫共沉淀技術(shù)(Co-IP)
-
05.14
四大研究利器(Co-IP、BIFC、Y2H、GST pull-down)助力速配蛋白互作“最佳拍檔”
-
05.14
高效、精準(zhǔn)、直觀、實(shí)時——取經(jīng)“蛋白互作研究翹楚”BIFC!
-
05.14
轉(zhuǎn)染效率低、干擾效果差、重復(fù)性欠佳...siRNA研究頻遇“攔路虎”怎么辦?
-
04.22
一文讀懂EMSA技術(shù)核心要點(diǎn),讓“emsa” 秒變“easy”
-
 在線客服
在線客服 -

 在線訂購
在線訂購 -

 掃碼領(lǐng)資料
掃碼領(lǐng)資料掃碼領(lǐng)資料

電話:19522948401
-

 文獻(xiàn)獎勵申請
文獻(xiàn)獎勵申請


