circRNA(circular RNA,環狀RNA)詳解
信息來源:金開瑞 作者:genecreate 發布時間:2022-11-01 10:12:29
近年來,circRNA作為非編碼RNA研究領域中的新寵,在每一個研究領域、研究方向都有發現circRNA新功能,吸引著無數科研小伙伴們的眼光聚焦于此,在心癢難耐、摩拳擦掌的同時,是不是又不知如何下手呢?嘻嘻,那偷偷告訴你呦,閱讀全文即可快速了解circRNA的前世今生和經典的研究思路。
簡介
circRNA(circular RNA,環狀RNA)是一類具有閉合環狀結構的非編碼RNA分子,沒有5′ 帽子結構和3′ poly(A)結構(如圖1),主要位于細胞質或儲存于外泌體中,不受RNA外切酶影響,表達更穩定且不易降解,已被證明廣泛存在于多種真核生物體內[1]。大多數circRNA是由外顯子環化而成,也有部分circRNA是由內含子環化而成的套索結構(lariat)。同時由于circRNA含有大量的miRNA應答原件(MREs),能與AGO蛋白形成RNA誘導沉默復合體(RISC)的催化核心,最終導致circRNA降解。根據來源,circRNA可大致分為四類:全外顯子型的circRNA,內含子和外顯子組合的EIcircRNA,內含子組成的套索型ciRNA,由病毒RNA基因組、tRNA、rRNA、snRNA等環化產生的circRNA。
圖1 circRNA結構示意圖 (Li et al., 2015)
研究背景
在二十年前,科學家們將從植物類病毒、酵母線粒體以及乙型肝炎病毒中鑒定的circRNA視為異常剪切后產生沒有調控功能的副產物。2013年,Nature雜志刊登了題為“Natural RNA circles function as efficient microRNA sponges”的circRNA研究文章,其首次提出并證實circRNA是作為miRNA海綿的調控機制,為circRNA研究提供了新的曙光。伴隨著RNA測序技術和生物信息分析的快速發展,在人組織的轉錄組中已經鑒定出14807個候選的circRNA,以及其他物種細胞中發現許多外顯子可被非線性的反向剪切或基因重排而形成circRNA。
《2018研究前沿》中,據統計circRNA已陸續榮登生物科學TOP10熱點榜單和新興前沿榜單,其細胞定位、成環機制和功能研究的熱度不減,儼然是非編碼RNA領域最火熱的明星分子。正如此,Han et al撰寫了一篇關于circRNA在各個疾病中研究進展的綜述,主要是探討其在未來腫瘤治療上優勢(如圖2),其中紅色的字體是腫瘤,黑色的字體是其它疾病[2],旨在為廣大科研學者們拋磚引玉。
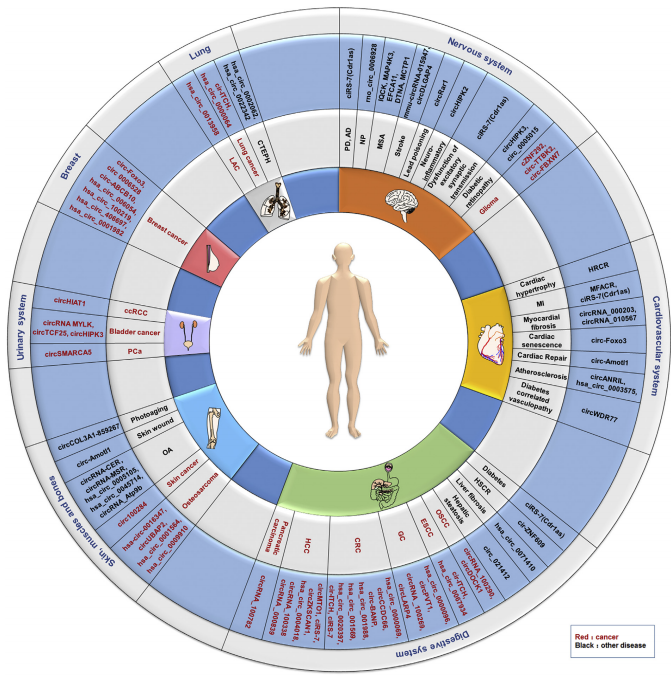
圖2 circRNA已被證實在不同疾病中的功能概述和研究進展(Han et al., 2018)
成環機制
circRNA環化方式分為內含子環化和外顯子環化[3],目前主流的成環機制可歸類成三種:
1. 依賴于剪切體的索尾插接環化。在mRNA前體上,通過連續的組裝小核核糖體蛋白從而催化外顯子下游的5′ 供體位點連接到上游的3′ 受體位點,索尾插接形成環化,然后通過剪切形成circRNA。
2. 順式作用元件促進circRNA形成。部分circRNA外顯子兩側的內含子中含有反向互補序列,首先在剪切位點上并排形成RNA雙鏈體,再通過可變剪切形成帶內含子和不帶內含子兩種不同的circRNA。或者外顯子內部以及兩側的內含子可以競爭進行RNA配對,最終通過可變剪切形成不同類型的circRNA。
3. RNA結合蛋白(RBPs)調控circRNA形成。通過將RBPs結合到外顯子側翼的內含子上,從而促進circRNA的形成[4-5]。

圖3 circRNA生物發生和調控機制圖(Chen et al., 2016)
生物學功能
circRNA主要存在于細胞質或外泌體中,具有組織特異性、疾病特異性、時序特異性及高穩定性等特征。近幾年,大量的研究表明circRNA在生物的生長發育、脅迫應答、疾病發生和發展等方面密切相關,并預測其在疾病診斷標記物等方面的應用前景,但其生物學功能在很大程度上仍然未知。目前認可度比較高的circRNA生物學功能,歸類如下[6](如圖4):
1. miRNA sponge。circRNA富含miRNA結合位點來充當miRNA海綿作用,阻止miRNA在3′ 非翻譯區與mRNA相互作用,進而間接調控miRNA下游靶基因的表達。
2.調控蛋白結合。circRNA通過與mRNA調節的結合蛋白(RBP)結合,進而改變剪接模式或mRNA穩定性。
3.調控基因轉錄。circRNA與RNA聚合酶Ⅱ相互作用并調節轉錄,或者EIcircRNA可與小核糖核蛋白互作用,再與RNA聚合酶Ⅱ結合。
4.編碼功能。circRNA雖然屬于非編碼RNA,但也有部分circRNA可被核糖體翻譯并編碼多肽,進而行使調控功能。
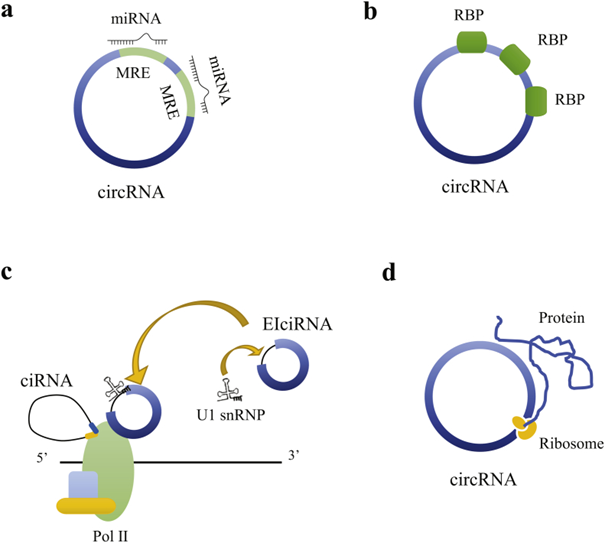
圖4 circRNA生物功能的調控機制圖(Zhang et al., 2018)
參考文獻
[1] Li Y., Zheng Q P., Bao C Y. Circular RNA is enriched and stable in exosomes: a promising biomarker for cancer diagnosis. Cell Res. 2015 Aug, 25(8): 981–984.
[2] Han B., Chao J., Yao H H. Circular RNA and its mechanisms in disease: From the bench to the clinic. Pharmacol. Ther. 2018 Jul, 187:31–44.
[3] Zhu L P., He Y J., Hou J C., et al. The role of circRNAs in cancers. Biosci Rep. 2017 Oct, 37: 5–12.
[4] Chen L L. The biogenesis and emerging roles of circular RNAs. Nat. Rev. Mol. Cell Biol. 2016 04, 17(4).
[5] Zhang Z R., Yang T T., Xiao J J. Circular RNAs: Promising Biomarkers for Human Diseases. EBioMedicine. 2018 Aug, 34: 267–274.
[6] Rong D W., Sun H D., Li Z X., et al. An emerging function of circRNA-miRNAs-mRNA axis in human diseases. Oncotarget. 2017 Sep 22, 8(42): 73271–73281.
相關技術服務
推薦閱讀
最新動態
-
09.23
中藥的現代詮釋:外泌體如何革新傳統醫學?
-
07.02
1+1>2!深度解析RNA測序數據挖掘邏輯和后期實驗設計思路,輕松研獲10+ SCI
-
07.01
“稻”亦有道——盤點近期水稻研究的重大突破
-
06.28
科學與美學的結合體:植物亞細胞定位技術詳解
-
06.28
“聚焦新質生產力,激發科研新動能”|LCA躋身蛋白互作研究的新銳力量
-
06.05
知無不“研”|一文讀懂免疫共沉淀技術(Co-IP)
-
05.14
四大研究利器(Co-IP、BIFC、Y2H、GST pull-down)助力速配蛋白互作“最佳拍檔”
-
05.14
高效、精準、直觀、實時——取經“蛋白互作研究翹楚”BIFC!
-
05.14
轉染效率低、干擾效果差、重復性欠佳...siRNA研究頻遇“攔路虎”怎么辦?
-
04.22
一文讀懂EMSA技術核心要點,讓“emsa” 秒變“easy”










